摘要: 很多癌症患者都关心MSI状态,会不会影响靶向药的效果?这篇文章给你讲清楚。MSI和靶向药其实是两套不同的“作战系统”,一个针对基因突变,一个利用免疫系统。别再把免疫治疗的成功案例当成靶向药的功劳了!搞清楚这个区别,才能选对治疗方案,不走弯路。
在肿瘤治疗领域,微卫星不稳定性(MSI)检测的普及率越来越高,大约15%-20%的结直肠癌患者和更多实体瘤患者会进行这项检测。一个经常被问到的问题是:MSI状态,会不会影响靶向药的效果? 这个问题的背后,其实藏着对两种核心治疗逻辑的混淆。今天,我们就来把这事儿掰扯明白。
先搞明白:MSI和靶向药,它俩到底管的是啥?
你得把肿瘤治疗想象成一场战争,不同的武器对付不同的敌人。
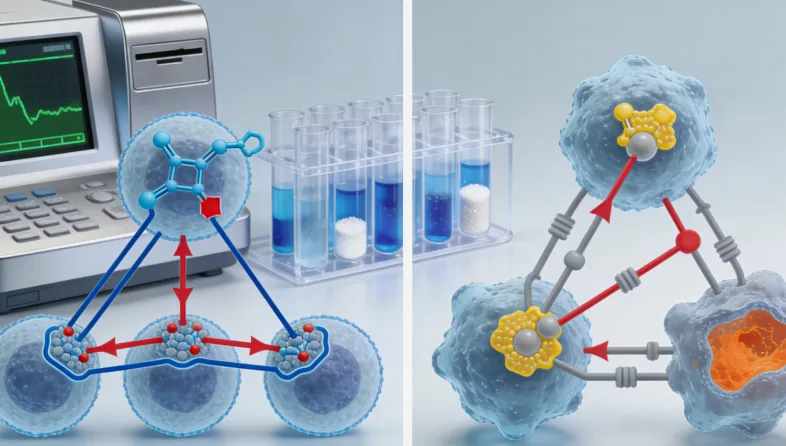
靶向药,是“精确制导导弹”。它的目标是肿瘤细胞上某个特定的“靶点”,比如EGFR、ALK、HER2这些由基因突变产生的异常蛋白。药的设计就是精准地结合上去,要么阻断信号,要么直接“毒死”细胞。前提是,你的肿瘤必须有这个靶点(基因突变),导弹才有地方瞄准。没有突变,用上靶向药基本就是“放空炮”,效果微乎其微。
MSI状态呢?它反映的不是一个具体的靶点,而是肿瘤细胞的“整体特征”。你可以把它理解为肿瘤细胞的“身份证bug”。正常细胞有一套完美的DNA复制纠错系统(错配修复功能,MMR)。MSI-H(高度微卫星不稳定)或dMMR(错配修复功能缺陷)的肿瘤,这套纠错系统坏了,复制时错误百出,产生一大堆新奇的、乱七八糟的蛋白质(新抗原)。
这些新抗原对免疫系统来说,就像插满了“小红旗”的异常细胞,特别容易被识别和攻击。所以,MSI状态本质上是预测免疫治疗效果的“风向标”,而不是靶向药的靶点。
看明白了吗?一个(靶向药)看的是“点”(单个基因突变),另一个(MSI)看的是“面”(基因组整体的不稳定性)。出发点完全不同。
关键来了:MSI状态,会不会影响靶向药的效果?
直接说结论:通常没有直接影响,但可能有间接的、复杂的关联。
1. 机制上不相关:决定靶向药疗效的核心是“驱动基因突变”是否存在。EGFR抑制剂只认EGFR突变,不管你是MSI-H还是MSS(微卫星稳定)。ALK抑制剂也只认ALK融合。MSI状态是另一条赛道上的事,它不改变这些靶点蛋白的结构和功能。所以,单纯从作用机制上讲,MSI状态,会不会影响靶向药的效果?答案通常是“不会”。
2. 但现实更复杂一点:肿瘤不是简单的模型。有些研究发现,在某些特定的癌种和靶点中,MSI状态和某些基因突变似乎“不太爱同时出现”。比如,在结直肠癌里,典型的RAS/BRAF突变和MSI-H状态就有一定的互斥性。这意味着,一个MSI-H的肠癌患者,他本身携带RAS/BRAF突变的概率就可能较低。而RAS/BRAF野生型,恰恰是使用西妥昔单抗(一种靶向药)获益的前提。你看,这不是MSI直接影响了靶向药效果,而是它可能和影响靶向药疗效的“其他基因”存在某种分布上的关联。这是一种间接的、统计学上的联系,并非因果。
3. “超进展”的罕见风险:极少数回顾性研究曾提示,存在dMMR/MSI-H的患者使用某些靶向药物(如EGFR抑制剂)时,发生肿瘤“超进展”(治疗期间肿瘤快速生长)的风险理论上可能增加,但这部分数据非常初步,争议极大,远未成为临床定论,绝不能作为常规治疗的依据。
所以,当你再思考“MSI状态,会不会影响靶向药的效果”时,要记住:医生决定用不用靶向药,首要依据是相应的基因检测报告(有没有靶点突变),MSI报告是放在旁边、用来规划另一条治疗路线(免疫治疗)的重要参考。
别搞混了!这些“神效”案例,其实不是靶向药的功劳
这里有个最常见的误解,必须单独拎出来讲。
临床上,偶尔会听到这样的故事:“一个晚期肠癌患者,用了某种药(比如瑞戈非尼、呋喹替尼等),效果特别好,一查原来是MSI-H!”
很多人下意识觉得:看,MSI-H让这个靶向药效果变好了!
大错特错。正确的解读应该是:这个患者之所以效果超群,很可能不是(或不仅仅是)靶向药本身的功劳,而是因为他MSI-H的体质,本身就对免疫治疗极其敏感。
目前的研究认为,某些多靶点抗血管生成的靶向药(比如上面提到的这类),除了抑制肿瘤血管生成,还可能具有调节肿瘤免疫微环境的作用。比如,它们能让原本“免疫荒漠”的肿瘤里,跑来更多的免疫细胞。对于一个本身就因为MSI-H而插满“小红旗”(新抗原)的肿瘤来说,一旦免疫细胞被“招募”进来,就能立刻识别并发动猛烈攻击,产生“1+1>2”甚至“如虎添翼”的协同效果。
这个惊人的疗效,是“免疫治疗”逻辑的胜利,而不是“靶向治疗”逻辑的常规体现。如果把功劳全算在靶向药头上,就会彻底误解MSI状态,会不会影响靶向药的效果这个问题的本质。这更像是免疫治疗潜力在特定条件下的“提前展现”或“被激发”。
那MSI高,我该用什么药?给你3点核心建议
聊了这么多,最后落到实际治疗上,如果你是MSI-H/dMMR的患者,到底该怎么规划治疗策略?
1. 优先考虑免疫治疗,这是你的“王牌”:对于晚期MSI-H/dMMR的实体瘤患者,PD-1抑制剂等免疫治疗是国内外指南公认的一线优选方案。它的原理与你的肿瘤特征完美匹配:肿瘤新抗原多 → 免疫细胞易识别 → PD-1抑制剂解除免疫细胞的“刹车” → 免疫系统全力攻击肿瘤。有效率远高于传统化疗,且可能获得长期生存。
2. 靶向药并非无用,但要“对因下药”:不要因为MSI-H就完全排斥靶向药。正确的做法是:该做的靶点检测一个都不能少。如果你同时存在明确的靶向药驱动基因突变(比如肺癌的EGFR突变),那么针对该突变的靶向药依然是重要且有效的选择。这时,你的MSI-H状态是额外的“好消息”,意味着在靶向药之后或耐药时,你还有一张强大的免疫治疗“底牌”。治疗顺序需要医生高超的排兵布阵。
3. 警惕“替代品”思维,检测务必做全:千万不要以为“MSI检测”可以替代“靶向基因检测”。这是两条必须平行进行的检测线。完整的肿瘤治疗规划,需要一份全面的基因检测报告,它既要告诉你有没有靶向药可用的“靶点”(如NGS测序),也要告诉你免疫治疗有没有戏(MSI/MMR、TMB等)。只做一个,都可能让你错失最佳的治疗机会。
说到底,MSI状态,会不会影响靶向药的效果?最准确的回答是:它不直接决定靶向药的疗效,但它是一把至关重要的钥匙,帮你打开了另一扇更可能通向长期生存的大门——免疫治疗。用好这把钥匙,同时握好其他武器(靶向药、化疗等),在专业医生的指导下制定组合策略,才是战胜癌症的聪明做法。
